- 환자 중심의 안전관리 체계 확립을 통한
- 국민 건강 보호 길라잡이
 입니다.
입니다.
장기추적조사계획이란?
장기추적조사 대상으로 지정 받은 첨단바이오의약품에 대하여 「약사법」 제34조제1항에 따라 임상시험계획 승인을 받은 자, 첨단바이오의약품 품목허가를 받은 자, 수입자는 장기추적조사 계획을 수립하여 식품의약품안전처장에게 제출해야 한다.
처리절차
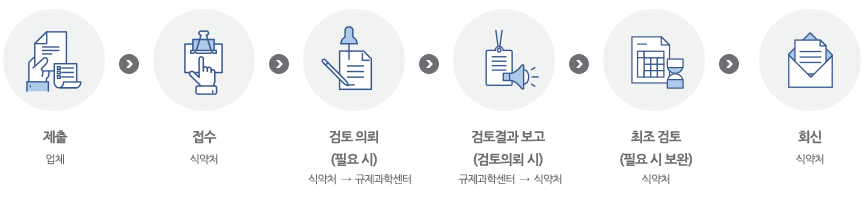
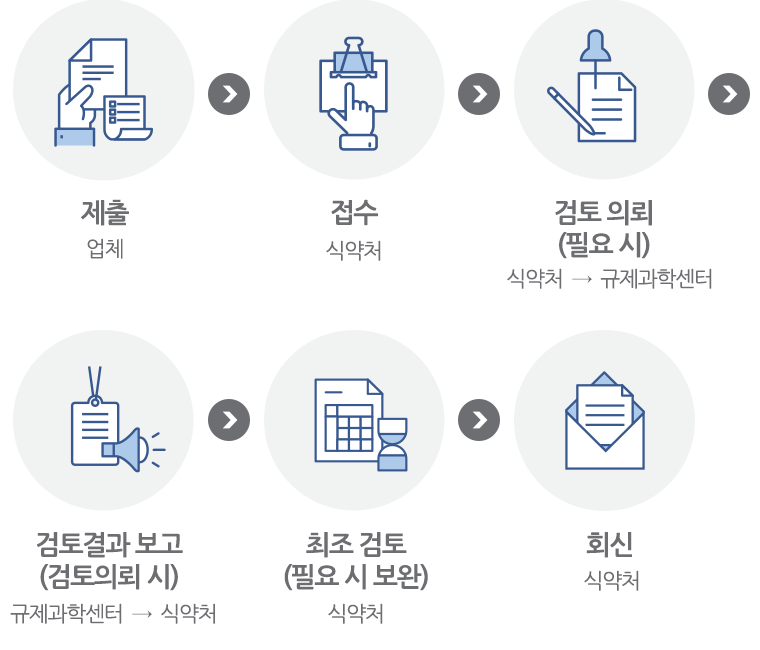
제출 대상자
장기추적조사 대상으로 지정받은 첨단바이오의약품에 대하여 「약사법」 제34조제1항에 따라 임상시험계획 승인을 받은 자,
첨단바이오이의약품 품목허가를 받은 자, 수입자
보고시기
임상시험계획 승인을 받은 자, 품목허가를 받은 자 또는 수입자는 장기추적조사 계획을 다음 각 호의 구분에 따른 날의 전날까지 수립하여 식품의약품안전처장에게 제출해야 한다.
1. 임상시험 계획 승인을 받은 자: 임상시험용 첨단바이오의약품을 공급한 날
2. 품목허가를 받은 자 및 수입자: 첨단바이오의약품을 판매˙공급한 날
(첨단바이오의약품 안전 및 지원에 관한 규칙 제32조제2항)
근거
첨단바이오의약품 장기추적조사 관리기준 제정고시
「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」(법률 제16556호, 2019.8.27. 제정) 시행(2020.8.28.)에 따라 인체세포 등으로 제조된 첨단바이오의약품에 대한 안전관리 강화를 위해 실시하는 장기추적조사에 대해 상위법령에서 위임한 세부 절차 및 방법을 정함으로써 장기추적조사를 적정하게 실시하고자 함
법률 내용
첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률 제30조제2항
첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률 시행령 제30조제1항
첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률 시행규칙 제32조
첨단바이오의약품 장기추적조사 관리기준 제3조,제4조,제5조


